来源: Nature Communications
来源: Nature CommunicationsNature Communications丨四川大学刘磊等团队一项Ⅱ期试验:局部晚期口腔鳞状细胞癌新辅助免疫化疗的疗效、安全性和单细胞分析
口腔鳞状细胞癌 (OSCC) 是非鼻咽头颈部鳞状细胞癌 (HNSCC) 最常见和最具挑战性的亚型。大约 60% 的 OSCC 患者在局部晚期被诊断为。目前可切除局部晚期 OSCC (LA-OSCC) 的标准治疗包括根治性手术切除后放疗或基于顺铂的同步放化疗。尽管如此,5 年总生存率仍低于 50%。此外,迄今为止的 III 期试验未能证明新辅助化疗对 LA-OSCC 的生存益处,这些都强调了对新治疗策略的迫切需求。
KEYNOTE048试验已确定免疫检查点抑制剂 (ICI) 单独使用或与化疗联合使用,作为不可切除的复发/转移性HNSCC的一线治疗。这促使进一步研究可切除HNSCC的此类策略,包括 LA-OSCC。正在进行的KEYNOTE689试验正在评估局部晚期HNSCC的2个周期新辅助mono-ICIs,最终结果待定。然而,在LA-OSCC中,新辅助单ICI治疗显示主要病理反应(MPR)率仅为 7.1%。
最近的I/II期试验显示,基于ICIs的联合疗法在局部晚期HNSCC(包括LA-OSCC)中具有潜在的生存获益,例如双重ICI、ICI加靶向治疗联合或不联合化疗、ICIs加放疗联合或不联合化疗,以及ICIs 联合化疗。其中,新辅助免疫化疗(NAIC)显示出极好的病理反应。临床前研究表明,在ICI中加入化疗可以增强抗肿瘤反应。NAIC已被确定为可切除非小细胞肺癌的标准治疗方法。然而,很少有临床试验专门在LA-OSCC患者中研究NAIC。
为了解决这一差距,四川大学刘磊等团队进行了一项单臂II期试验,以评估NAIC在2个周期的卡瑞利珠单抗加白蛋白结合型紫杉醇和顺铂治疗可切除LA-OSCC 患者中的疗效和安全性。还探讨了LA-OSCC 中NAIC反应的潜在生物标志物和潜在机制。
2025年4月28日,Nature Communications上发表四川大学刘磊等团队题为“Efficacy,safety and single-cell analysis of neoadjuvant immunochemotherapy in locally advanced oral squamous cell carcinoma:a phase II trial ”的研究论文,在这项试验中,卡瑞利珠单抗联合白蛋白结合性紫杉醇和顺铂的NAIC在LA-OSCC患者中显示出良好的病理反应和可控的安全性。通过scRNA-seq、scTCR-seq、mIF分析和实验证明,确定了基线CD4_Tfh_CXCL13细胞作为NAIC反应的潜在预测生物标记物。

在 2023年2月 日至2024年5月31日期间,筛选了35名患者,并入组了33名患者。两名患者在开始NAIC之前撤回了同意。因此,共有31名患者接受了NAIC。平均年龄为54±11岁,27例患者 (87.1%) 为男性。大多数患者(58.1%,18/31) 为临床IVA期疾病。
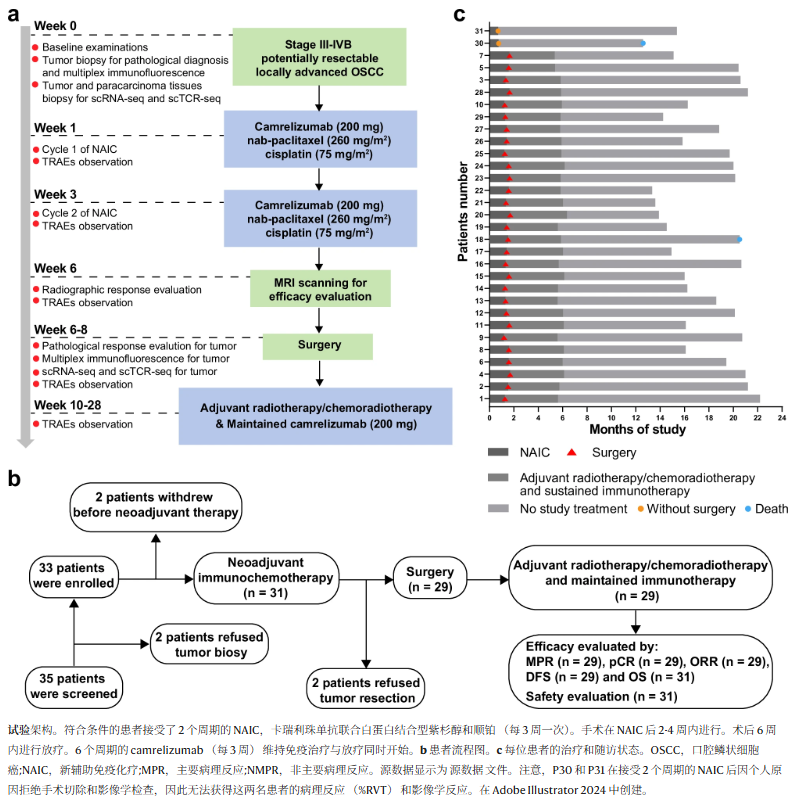
所有31例患者都完成了2个周期的NAIC。其中2例患者因个人原因拒绝手术切除和影像学检查。因此,29例患者(93.5%)接受了根治性手术。这29例患者随后均接受术后放疗或放化疗和免疫治疗作为维持治疗。每位患者的治疗程序、研究流程图和随访状态如图 1 所示。
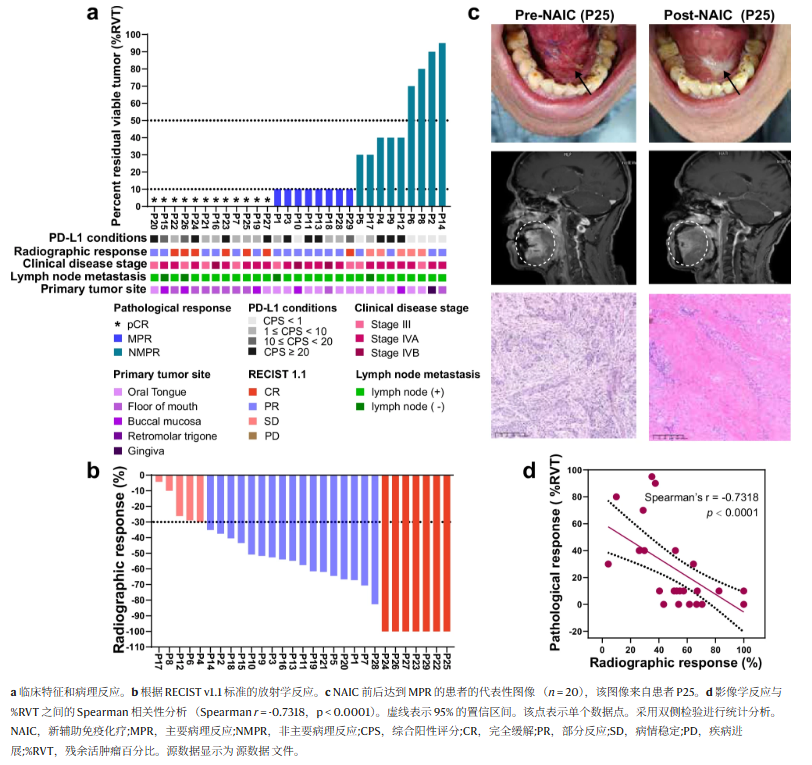
共有29例接受手术的患者可评估病理反应和影像学反应。MPR率为69.0%(20/29,95%CI: 49.2–84.7%),病理完全缓解(pCR)率为41.4%(12/29, 95%CI:23.5–61.1%)(图 .此外,所有3例基线IVB期疾病患者均在原发肿瘤和颈部淋巴结中均达到MPR。在26例基线III/IVA期疾病患者中,17例原发肿瘤达到MPR(包括11例pCR),14例颈部淋巴结达到MPR(包括8例pCR)。所 MPR患者在NAIC后均出现原发肿瘤的病理下期。根据RECISTv1.1的ORR为82.8%(24/29,95%CI: 64.2–94.2%)。NAIC后,7名患者达到完全缓解,17名达到部分缓解,5名病情稳定,没有患者出现疾病进展(图2b). NAIC前后的代表性放射学反应和病理反应图像如图2所示。2c.观察到放射学反应与残留活肿瘤百分比(%RVT)之间存在显着相关性(Spearman的r= − 0.7318,p < 0.0001)(图 D)2d)。
截至2024年11月30日数据截止日,31名接受治疗的患者的中位随访时间为18.6个月(范围:12.6-22.2)。对于所有31名接受治疗的患者,18个月的OS概率为96.77%(95% CI:79.23-99.54%)(补充图对于NAIC后拒绝手术的2例患者,1例 cT4bN2aM0)未接受任何后续治疗,在初始研究治疗后12.6个月死亡。另一名患者(cT4bN1M0)在NAIC后在当地医院接受了MRI复查,表明完全缓解。患者随后在当地医院接受放疗,但在初始研究治疗后14个月出现颈部淋巴结转移。对于29名接受手术的患者,18个月无病生存概率为85.71%(95%CI:53.95-96.22%)(补充图 1)).
本研究是迄今为止评估基于ICIs的新辅助治疗对LA-OSCC疗效的最大规模试验(n= 29)。以前的研究报道了局部晚期HNSCC的病理反应。例如,新辅助单/双ICB(MPR率:5.9-35%;pCR率:0-10%)、ICB 联合靶向治疗±化疗(MPR率:40-60%;pCR率:5-40%)、ICB联合放疗±化疗(MP 率:43-60%;pCR率:20-57%;包括p16阳性患者)和ICB 联合化疗(MPR率:27.8-74.1%;pCR率:16.7–55.6%),等等。与这些结果相比,本研究中卡瑞利珠单抗联合白蛋白结合型紫杉醇和顺铂的方案似乎显示出相当的病理反应率,MPR率为 69%,pCR率为 41.4%。此外,本研究中2个周期的NAIC达到的MPR率 (69%) 与局部晚期HNSCC中相同方案的3个周期(63%)相当。
在这项研究中,卡瑞利珠单抗联合白蛋白结合型紫杉醇和顺铂的新辅助方案耐受性良好,在NAIC期间没有发生意外的TRAE。只有2例患者在 NAIC期间出现≥3级TRAE,均在对症治疗后消退。值得注意的是,在本研究中,使用2周期NAIC观察到的反应性皮肤毛细血管内皮增生的发生率低于使用相同方案的3周期NAIC观察到的反应性皮肤毛细血管内皮增生的发生率(16.1% vs. 29.2%)。此外,本研究中≥3级TRAEs的发生率低于 Illuminate试验中报告的发生率 (6.4% vs. 15%)。这些结果突出表明需要进一步研究NAIC循环的最佳数量,以实现LA-OSCC患者降低毒性和良好疗效之间的平衡。此外,手术并发症是口腔颌面外科医生的一个关键问题,与传统的标准根治性切除术相似。
确定LA-OSCC中基于ICIs的新辅助治疗的预测生物标志物仍然具有挑战性。而PD-L1表达被推荐作为复发性和转移性HNSCC免疫治疗的治疗指标。本研究观察到PD-L1表达与%RVT之间无显著相关性。这种差异可能是由于NAIC前活检样本中PD-L1评估的准确性有限。此外,我们发现MPR和 NMPR患者之间的基因表达没有显著差异,而较高的TMB水平与对NAIC的病理反应改善相关。
总之,新辅助卡瑞利珠单抗联合白蛋白结合型紫杉醇和顺铂在LA-OSCC患者中显示出有希望的病理反应和可接受的安全性。进一步的探索性分析表明,CD4_Tfh_CXCL13细胞是NAIC的重要预测生物标志物,这可能有助于确定最有可能从治疗方案中受益的患者。该研究结果可能为III期试验的进一步验证提供临床和理论见解。
原文链接:https://www.nature.com/articles/s41467-025-59004-w#Sec16
图片来源网络如有侵权请及时联系删除!