来源: advanced science
来源: advanced scienceAdv Sci|天津医科大学李晓青等团队揭示成骨细胞微环境决定了骨髓中传播的乳腺癌细胞的命运!
骨骼是转移性乳腺癌细胞最常见的归宿。骨微环境在决定已扩散至骨髓的癌细胞命运中起着关键作用。支持性的微环境促进癌细胞在骨骼内的存活和增殖,促进早期骨转移的发展。相反,不合适的骨骼微环境可能导致癌细胞静止,直到微环境变化促使休眠癌细胞觉醒,形成晚期骨转移。
静止肿瘤细胞可以作为单个散布肿瘤细胞(DTCs),处于长期休眠状态且G0/G1停止,或作为小簇微转移细胞在增殖与凋亡之间保持平衡,不会导致净大小变化。从单一DTC向骨微转移的进展代表了骨溶解前骨骼定殖的关键早期阶段。
重要的是,静止期是一个未被充分利用的治疗窗口,可以介入并消除DTC和微转移,因为传统化疗和放疗方法对这些周期缓慢的细胞群体疗效有限。因此,研究骨髓中癌细胞定植、休眠维持和再觉醒的机制,可能为潜在治疗靶点提供支持。
2026年2月6日,天津医科大学李晓青团队在Advanced Science上发表题为"The Osteoblastic Microenvironment Determines the Fate of Breast Cancer Cells Disseminated in the Bone Marrow"的论文,这项研究揭示了成骨细胞微环境如何决定骨髓中癌细胞的命运。

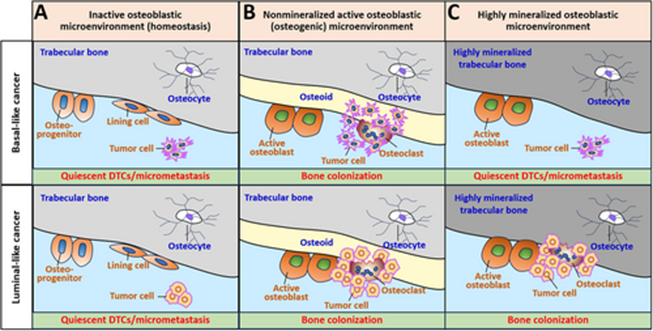
本研究揭示了成骨微环境如何决定骨髓内播散肿瘤细胞的最终命运:
1.在处于稳态的静止型成骨微环境中,肿瘤细胞会以播散肿瘤细胞(DTCs)或微转移灶的形式维持静息状态;
2.在活跃的非矿化成骨微环境(成骨生成阶段)中,肿瘤细胞会快速定植于骨骼。
3.在高矿化程度的成骨微环境中,基底样乳腺癌细胞会维持静息状态,而管腔样乳腺癌细胞则能够存活并侵袭骨组织。
在成人正常生理条件下,骨骼稳态反映了一个非活跃的成骨细胞微环境,这种微环境由成骨与骨溶解之间的微妙平衡维持。在此背景下,成骨细胞微环境由矿化骨基质和非活性成骨细胞组成,这些细胞主要作为非活跃的衬里细胞和前驱细胞存在,同时还嵌入骨基质中的末端分化骨细胞。
本研究观察到基底样癌细胞作为小鼠稳态骨中的DTCs或微转移细胞保持静止,体外实验证实其在非活跃的成骨细胞微环境中缓慢增殖。由于E2不可避免地激活成骨细胞微环境,而E2对癌细胞生长至关重要,我们无法在小鼠体内复制类腔管状癌细胞的状态,但在体外非活性的成骨细胞条件下,腔腔类细胞同样表现出缓慢的增殖。这些体内和体外的综合结果表明,在稳态期扩散到非活性成骨细胞微环境中的肿瘤细胞,通常会以DTC或微转移的形式进入静止状态(见下图2)。
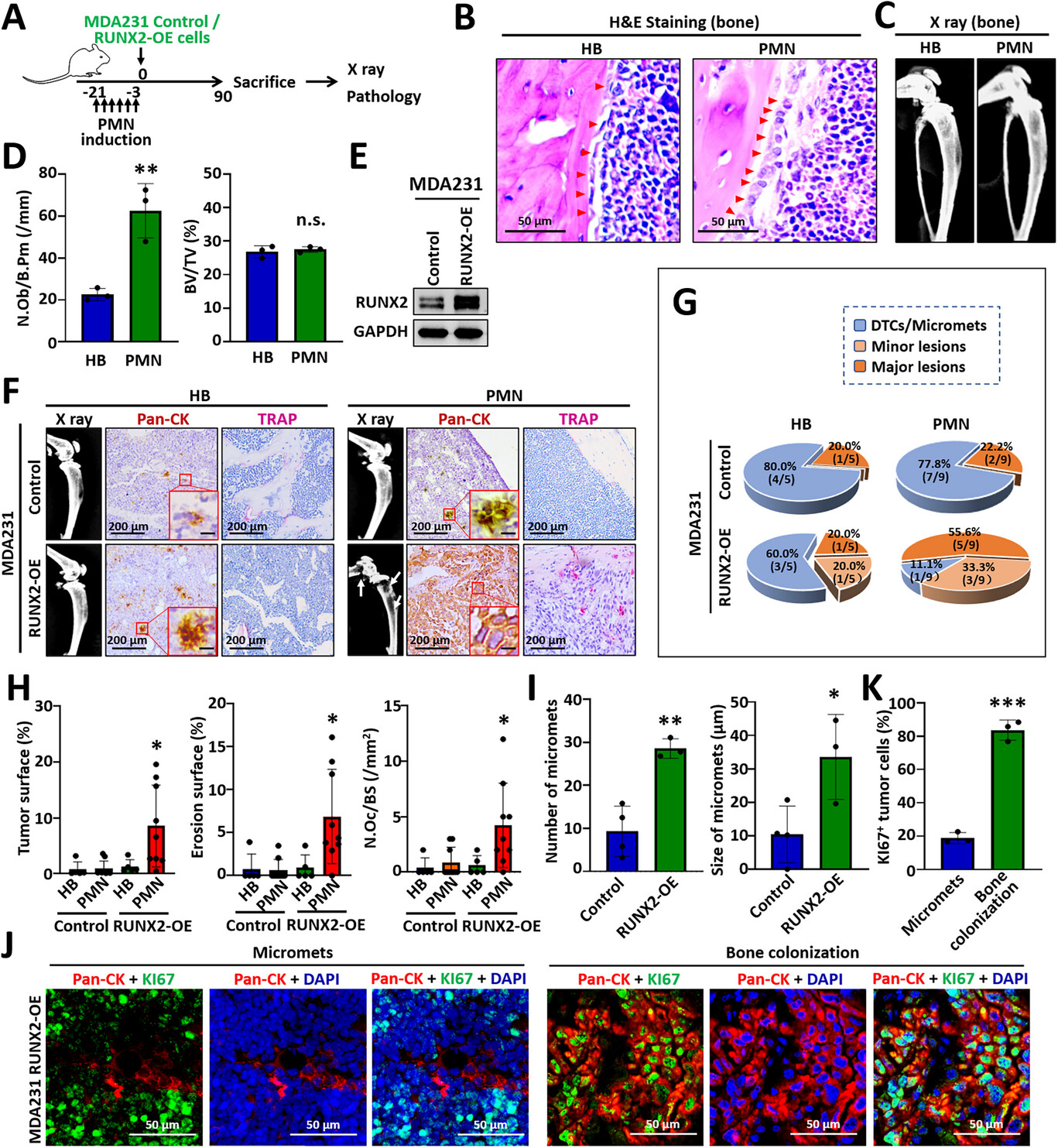
Runt相关转录因子2(RUNX2)是成骨分化过程中的核心转录因子,在嗜骨性乳腺癌细胞中高度富集,具有显著促进骨转移的能力。我们此前的研究发现,高表达RUNX2的乳腺癌细胞可作为嗜骨性“种子”,被成骨细胞招募,并在活跃的成骨性转移前微环境(PMN)中定植于骨组织。但这类高表达RUNX2的肿瘤细胞在正常小鼠体内的骨组织中并不具备生存或定植优势。由于成骨细胞谱系涵盖多种细胞状态,从静息的成骨前体细胞、骨衬细胞到成熟成骨细胞及终末分化的骨细胞,我们推测成骨微环境的分化状态可能是决定骨髓内肿瘤细胞命运的关键因素。
在成年女性体内,成骨微环境的分化状态与骨密度受激素、细胞因子、维生素D及钙摄入的系统性调控。雌激素是骨量的主要保护因素之一,通过促进成骨细胞的骨形成作用、抑制破骨细胞介导的骨吸收过程来维持骨密度。甲状旁腺激素(PTH)对维持钙稳态与骨稳态至关重要:其可同时调控骨形成与骨吸收,短期低剂量使用时主要促进成骨细胞分化,增加骨形成。人PTH的N端片段PTH(1-34)可将成骨前体细胞与静息骨衬细胞转化为成熟成骨细胞,因此已被批准用于骨质疏松的治疗。钙是骨代谢的核心物质,可为骨矿化提供必需的矿质原料:饮食钙摄入不足会阻碍骨矿化进程,导致未矿化骨基质(类骨质)异常堆积。此外,长期大剂量使用地塞米松(DEX)等糖皮质激素会抑制定型成骨细胞的成熟与功能。
在本研究中,我们通过联合使用不同剂量的PTH、雌激素,搭配低钙饮食与地塞米松处理,构建了多种特征明确的成骨微环境模型。随后以过表达RUNX2的乳腺癌细胞作为嗜骨性“种子”,系统探究了成骨微环境的分化状态如何调控骨髓内播散肿瘤细胞的命运。本研究针对播散肿瘤细胞在骨组织中的不同结局——即快速定植、以播散肿瘤细胞或微转移灶形式维持静息,以及从休眠状态再次激活——给出了系统性解释;阐明了成骨微环境的细胞组分(成骨细胞)与基质组分(骨基质)在乳腺癌骨定植过程中的不同作用。此外,我们通过动物实验评估了靶向阻断肿瘤细胞与骨基质之间整合素介导的相互作用的治疗潜力,为抑制休眠肿瘤细胞的再次激活及骨定植提供了新的干预思路。
上述发现针对播散肿瘤细胞在骨组织中的不同结局——即快速定植、长期休眠或是从休眠状态再次激活,给出了系统性的解释。此外研究证实,在具有转移促进性的成骨微环境中,肿瘤细胞与分化成熟的成骨细胞均可激活破骨细胞,最终引发溶骨性骨损伤。成骨细胞(细胞组分)与骨基质(基质组分)在骨转移定植过程中分别发挥了不同作用。研究还通过动物实验评估了靶向整合素介导的肿瘤细胞-骨基质相互作用的治疗潜力,该疗法可有效抑制静息状态肿瘤细胞的复苏及骨定植能力。
原文参考:https://doi.org/10.1002/advs.202509980
备注:图片来源网络如有侵权请及时联系删除!